
A promessa dos novos testes
Domingos Zaparolli
Pesquisadores brasileiros desenvolvem seis exames para detecção do Sars-CoV-2 a partir de amostras de saliva
Os últimos meses foram pródigos em anúncios de novos kits diagnósticos para a Covid-19. Institutos de pesquisa, startups e laboratórios brasileiros lançaram ou informaram que estão perto de lançar seis novos testes para detectar a presença do Sars-CoV-2 a partir da saliva dos pacientes. Com isso, os desenvolvedores pretendem eliminar o sistema invasivo de coleta de amostras utilizado no teste RT-PCR (transcrição reversa seguida por reação em cadeia de polimerase), considerado o padrão ouro em diagnósticos da doença. O RT-PCR gera desconforto ao utilizar swabs – uma haste longa, semelhante a um cotonete, com aproximadamente 15 centímetros (cm) – para a coleta de secreções do fundo da garganta e do nariz, e expõe ao risco de contágio os profissionais da saúde que realizam o exame. Outra preocupação dos pesquisadores é aliar respostas rápidas, praticidade, confiabilidade e custos acessíveis, elevando a oferta de testes para a população. Não é certo, contudo, que esse objetivo será atingido, pois alguns kits ainda não concluíram sua fase de desenvolvimento. Entre os que já foram finalizados ainda há incertezas se serão fabricados em larga escala.
No fim de 2020, o Centro de Estudos do Genoma Humano e Células-Tronco da Universidade de São Paulo (CEGH-CEL-USP) disponibilizou um ensaio, batizado de RT-Lamp Direto, capaz de diagnosticar a Covid-19 pela saliva. Segundo a bióloga e geneticista Maria Rita Passos-Bueno, coordenadora do projeto, a técnica molecular RT-Lamp (transcrição reversa seguida por amplificação isotérmica mediada por alça) demanda a realização de uma transcrição reversa (RT), na qual o RNA (ácido ribonucleico) é transformado em DNA (ácido desoxirribonucleico) para se obter a informação genética do vírus. Posteriormente, há uma etapa de amplificação, em que regiões específicas da amostra são replicadas milhões de vezes para que a presença do patógeno possa ser identificada.
Esses dois processos são semelhantes ao que ocorre no diagnóstico por RT-PCR. A diferença é que este exige a extração do RNA do vírus e isso demanda uma equipe especializada e reagentes químicos importados. “É uma etapa demorada, laboriosa, envolve a manipulação de material contagioso, e tem custo relativamente alto”, descreve Passos-Bueno. O teste do CEGH-CEL, desenvolvido com apoio da FAPESP, dispensa a etapa de extração do RNA. A técnica promove o rompimento por aquecimento do capsídeo – a estrutura de moléculas proteicas que reveste o núcleo do vírus – e a adição de uma solução química que estabiliza o vírus para a conversão do RNA viral em DNA.
O CEGH-CEL não é o primeiro a realizar ensaios com a técnica RT-Lamp no Brasil. A Universidade Federal de Goiás (UFG) desenvolveu um teste similar e o laboratório de genômica Mendelics, de São Paulo, já comercializa um ensaio parecido. A contribuição da equipe da USP, segundo a pesquisadora, foi desenvolver reagentes nacionais para o processo. “Elaboramos uma solução química que libera o RNA do vírus presente na saliva, aumenta sua estabilidade e garante um resultado eficiente”, afirma. Um acordo com o Instituto de Química da USP garantiu a produção local dos reagentes e principais insumos.
De acordo com os dados atuais, a sensibilidade do diagnóstico utilizando reagentes comerciais, ou seja, a capacidade de identificar o vírus em pacientes contaminados, é de 94% no período de infecção ativa, o que significa que 6% dos exames podem registrar falsos negativos. A especificidade, isto é, sua capacidade de identificar os indivíduos não contaminados, é de 99% – a taxa de falso positivo, portanto, é de apenas 1%. No momento, o CEGH-CEL realiza o exame em qualquer pessoa que procure a instituição, com ou sem sintomas de Covid-19. Ele fica pronto em 24 horas e custa R$ 90. O laboratório estuda parcerias para transformar o teste em um produto comercial para um público mais amplo. Um diagnóstico RT-PCR em São Paulo custa entre R$ 320 e R$ 400 e o resultado sai em 48 horas.
Em uma fase comercial mais avançada está a solução de diagnóstico desenvolvida pelo laboratório DNA Consult Genética e Biotecnologia, de São Carlos (SP), que também coleta a amostra por meio de saliva para fazer um exame denominado PCR em Tempo Real. Segundo o diretor científico, Euclides Matheucci Junior, o ensaio, desenvolvido em parceria com o Departamento de Genética Evolutiva da Universidade Federal de São Carlos (UFSCar), é realizado por meio da análise dos segmentos N1 e N2 do genoma do Sars-CoV-2, que codificam a proteína que encapsula e protege o material genético do vírus, e do gene humano RNase P. O teste tem eficácia equivalente à do RT-PCR, de acordo com a empresa. “Realizamos diagnósticos para prefeituras, planos de saúde e particulares na região de São Carlos e Grande São Paulo”, informa Matheucci. O valor do diagnóstico, que leva 24 horas para ser processado, é de R$ 240.

Biossensores
O uso de biossensores é outra estratégia para aperfeiçoar o diagnóstico da Covid-19. O Instituto de Física de São Carlos (IFSC), também da USP, desenvolve uma técnica que tem como base um genossensor, um dispositivo elaborado com nanotecnologia para detectar material genético. Conforme explicação do físico Osvaldo Novais de Oliveira Junior, do IFSC-USP e coordenador do projeto, o genossensor é composto de uma camada extremamente fina de uma sequência de DNA do Sars-CoV-2 sobre uma matriz – também de dimensões nanoscópicas – depositada sobre uma lâmina de vidro recoberta com trilhas ou nanopartículas de ouro. “A detecção do vírus ocorre quando a sequência de DNA reconhece uma sequência complementar de DNA na amostra sob análise, que mimetiza o RNA do Sars-CoV-2”, detalha o pesquisador.
Segundo Oliveira Junior, sua equipe fez a detecção da sequência do DNA imitando o RNA de quatro maneiras distintas e demonstrou que diferentes técnicas servem para essa tarefa. “O genossensor foi planejado para ser uma alternativa ao RT-PCR, pois também permite a detecção do material genético do vírus. A vantagem é que o teste pode ser feito em 30 minutos, sem a necessidade de análise em laboratório e apresenta um custo unitário inferior a R$ 10”, informa o pesquisador. A expectativa é que o diagnóstico por genossensores, que deve usar a saliva dos pacientes como amostra, apresente um índice de acerto semelhante ao do RT-PCR. O exame ainda está em fase de desenvolvimento e precisa ser testado em infectados.
O Laboratório de Genômica e Bioenergia da Universidade Estadual de Campinas (LGE-Unicamp) e a startup BIOinFOOD também trabalham em uma técnica que utiliza um biossensor para detectar a infecção pelo Sars-CoV-2. O teste denominado CoronaYeast utiliza a levedura Saccharomyces cerevisiae como base. Como explica o coordenador do projeto, Gonçalo Amarante Pereira, do Departamento de Genética e Biologia Molecular da Unicamp, na presença da proteína spike do novo coronavírus a levedura mudar de cor em poucas horas, saindo do bege para um verde fluorescente.
A amostra humana é coletada na saliva. “O sistema deverá ser sensível às mutações do vírus, que sempre vai ajustar a sua estrutura para continuar interagindo com a proteína ACE2, receptora do Sars-CoV-2 no organismo humano, e causar a doença”, detalha o pesquisador. O desenvolvimento do diagnóstico está na fase pré-clínica e ainda deve levar algum tempo até que seja lançado. “Acreditamos que será um teste rápido capaz de concorrer com o RT-PCR com um preço bastante reduzido se for produzido em larga escala”, informa Pereira. A equipe da Unicamp recebeu apoio da FAPESP para desenvolver o ensaio.
Estágio avançado
O Centro de Tecnologia da Informação Renato Archer (CTI), em Campinas (SP), trabalha no desenvolvimento de dois testes que utilizam uma base sensora eletroquímica descartável fabricada em uma placa de circuito impresso contendo nanoestruturas de óxido de zinco. Os dois testes estão sendo projetados para detectar em tempo real o Sars-CoV-2 nos primeiros dias de infecção utilizando como amostra a saliva da pessoa.
Um teste chamado de imunossensor emprega um anticorpo da proteína spike do vírus, que é imobilizado nas nanoestruturas do sensor e gera um sinal elétrico ao se ligar à proteína recombinante spike presente na saliva. O outro, denominado polímero impresso com vírus (VIP), utiliza uma camada polimérica para produzir um molde do vírus. Quando uma amostra contaminada entra em contato, o vírus se encaixa no molde, como nos brinquedos tipo Lego, alterando o sinal elétrico medido.
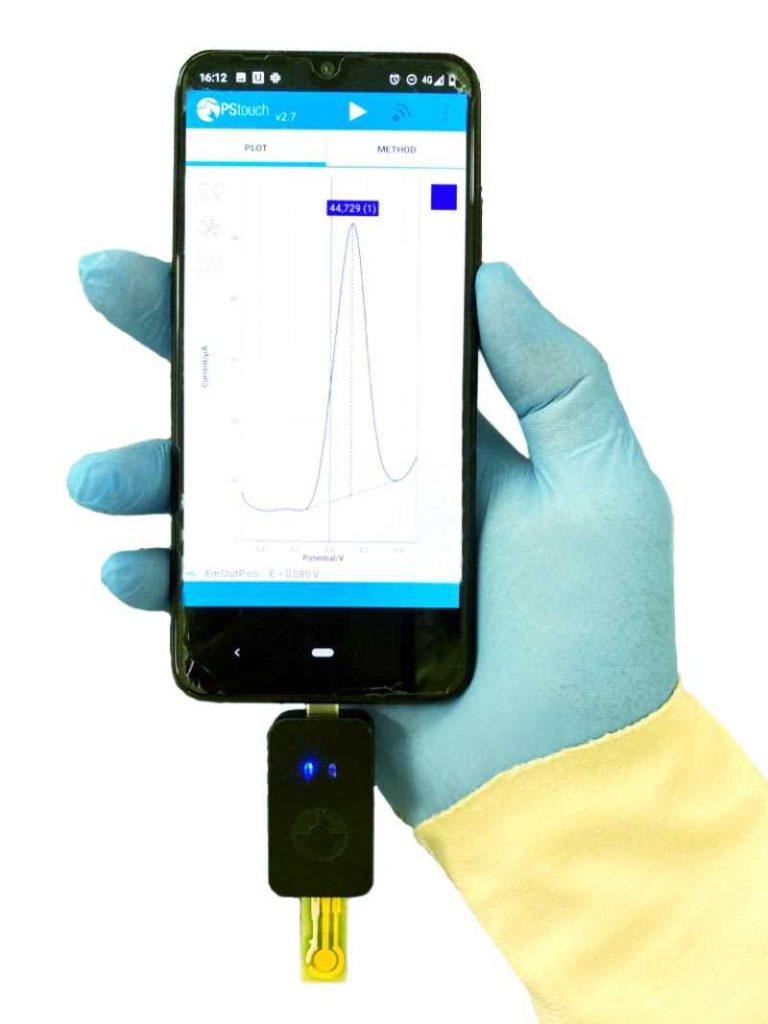
“Essas variações no sinal elétrico podem ser medidas com um equipamento portátil acoplado a um celular. Por isso, não demanda mão de obra especializada”, diz a pesquisadora Talita Mazon, coordenadora dos projetos no CTI, destacando que o teste é realizado diretamente na saliva.
O imunossensor vai passar por ensaios com as novas cepas do patógeno. Diante da cepa original, a eficácia constatada é de 94% em avaliações que estão sendo realizadas em ambiente hospitalar. O imunossensor é resultado de uma parceria do CTI com a startup paulista Visto.Bio, que já busca parceiros para a produção em escala dos testes. “O custo de produção deve ficar em torno de R$ 6. Poderá ser um teste prático, preciso e acessível”, avalia a pesquisadora.
Brasil é 120o colocado no ranking de testes
Reduzido número de diagnósticos dificulta o controle da pandemia no paísA população brasileira está entre as que menos realizam testes para diagnosticar a infecção pelo novo coronavírus. Em 9 de março, a plataforma internacional Worldometers, que colhe dados regionais e nacionais para divulgar diariamente a evolução do coronavírus no mundo, indicava o Brasil como o terceiro país em registro de casos, com 10,8 milhões de infectados, mas apenas na 120a posição em relação à realização de exames em sua população, com a testagem de 134 mil pessoas por milhão de habitantes.
Mesmo com o início da vacinação, os exames diagnósticos continuarão necessários. “É um vírus que ainda circulará por muito tempo entre humanos e provavelmente precisaremos de vacinações anuais, como ocorre com a gripe”, contextualiza a professora de ciências farmacêuticas da Universidade Federal de Minas Gerais (UFMG), Ana Paula Fernandes, coordenadora de diagnósticos da Rede Vírus do Ministério da Ciência, Tecnologia e Inovações (MCTI).
Em sua avaliação, o número reduzido de testes no Brasil em comparação com outros países decorre de uma série de fatores, sendo o principal deles a baixa oferta de testagem por parte do setor público, que não faz um trabalho preventivo para rastreamento dos casos e contatos assintomáticos, isolamento e prevenção de transmissão, e só avalia indivíduos com sintomas expressivos da doença, quando a transmissão já ocorreu potencialmente para outros indivíduos. “Resta à população recorrer aos testes privados, que são caros, inacessíveis para a maior parte das pessoas e nem sempre eficientes”, lamenta.
Além dos exames moleculares RT-PCR, outro sistema tradicional de testes é por sorologia, que identifica a presença dos anticorpos IgG e IgM em amostras de sangue. A existência de anticorpos, porém, indica que o indivíduo já teve contato com o vírus, mas não é capaz de identificar a presença do vírus no organismo atestando a infecção. Nos primeiros 20 dias após o contágio por Covid-19, o contaminado ainda não gerou anticorpos. Nesse período, o teste por sorologia tenderá a apresentar um diagnóstico classificado como falso negativo. “Saber se a pessoa possui anticorpos é uma informação importante, mas o teste não retrata o momento atual e não permite avaliar a transmissibilidade”, diz Fernandes.
Existem várias técnicas de testes sorológicos. Uma das mais usuais emprega o ensaio imunoezimático do tipo Elisa, usado na maioria dos exames de sangue laboratoriais. O preço varia entre R$ 150 e R$ 200 em São Paulo. Há também os diagnósticos rápidos que utilizam um sistema idêntico aos testes de gravidez vendidos em farmácia, em que uma substância dentro de um pequeno módulo plástico muda de cor, identificando os anticorpos. “Além de não serem adequados para identificar a presença do vírus, muitos desses testes utilizam reagentes químicos de baixa qualidade, comprometendo até mesmo a identificação ou não de anticorpos”, alerta Fernandes.
Projetos
1. Diagnóstico molecular rápido, eficaz e de baixo custo da Covid-19 e estratégias para testagem populacional em larga escala (nº 20/05949-2); Modalidade Auxilio a Pesquisa ‒ Regular; Pesquisadora responsável Mayana Zatz (USP); Investimento R$ 183.930,00.
2. Rumo à convergência de tecnologias: De sensores e biossensores à visualização de informação e aprendizado de máquina para análise de dados em diagnóstico clínico (nº 18/22214-6); Modalidade Projeto Temático; Pesquisador responsável Osvaldo Novais de Oliveira Junior (USP); Investimento R$ 4.941.869,56.
3. Padrões coloridos baseados em cristais fotônicos bioinspirados para aplicações mecanocromáticas (nº 20/02938-0); Modalidade Bolsa de Pós-doutorado; Pesquisador responsável Osvaldo Novais de Oliveira Junior (USP); Investimento R$ 203.497,56.
4. CDMF ‒ Centro de Desenvolvimento de Materiais Funcionais (nº 13/07296-2); Modalidade Centros de Pesquisa, Inovação e Difusão (Cepid); Pesquisador responsável Elson Longo (USP); Investimento R$ 47.007.381,97.
CDMF
O CDMF é um dos Centros de Pesquisa, Inovação e Difusão (Cepids) apoiados pela Fundação de Amparo à Pesquisa do Estado de São Paulo (Fapesp), e recebe também investimento do Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), a partir do Instituto Nacional de Ciência e Tecnologia dos Materiais em Nanotecnologia (INCTMN).




